がん治療(標準治療)の基礎知識
治療の流れを理解し、より適切な治療を受けるために
第18回 皮膚がん(悪性黒色腫、有棘細胞がん、基底細胞がん、乳房外パジェット病)
皮膚がんには多くの種類が存在する
皮膚を構成する細胞が悪性化したものを「皮膚がん」と総称しています。皮膚は外側から、表皮、真皮、脂肪層という部分に分かれています。そして、表皮はさらに、角層、顆粒層、有ゆうきょくそう棘層、基底層に分かれています(図1)
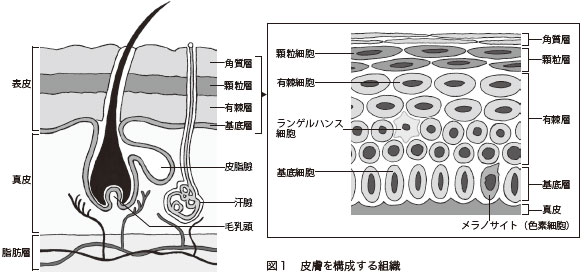
皮膚がんの多くは、表皮の細胞から発生し、増殖していきます。皮膚のどの細胞が悪性化して発生したかによって、皮膚がんにはいろいろな種類があります(図2)。
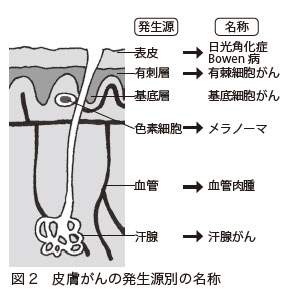
主なものは、悪性黒色腫(メラノーマ)、有棘細胞がん、基底細胞がん、乳にゅうぼうがい房外パジェット病の4つです。ここでは、この4種類の皮膚がんについて解説していきます。それぞれのがんの発生割合は、悪性黒色腫が2割程度、有棘細胞がんが3割程度、基底細胞がんが3割程度、乳房外パジェット病とその他の皮膚がんが2割程度です。
【悪性黒色腫】
日本人の悪性黒色腫は手足にできやすい
悪性黒色腫は表皮に存在するメラノサイトという色素細胞が、がん化することで発生します。メラノサイトは皮膚の色に関係するメラニンという色素をつくる細胞です。基本的には皮膚に発生するがんですが、口腔粘膜や鼻粘膜など、粘膜にできることもあります。
新悪性黒色腫には、表在拡大型、末端黒子型、悪性黒子型、結節型という4つのタイプがあり、日本人と欧米人では、できやすいタイプが違っています。
日本人に多いのは末端黒子型で、手や足などの部位によくできます。爪にできることもあります。高齢者に多いですが、若年者にも発症するのが特徴です。
一方、欧米人に多いのは表在拡大型で、これは主に体幹部にできます。日光に当たらない部位にできるため、このタイプの発生には紫外線が関係していないと考えられています。
悪性黒色腫は、ほくろと見分けがつきにくいことが多いので、中年以降に露出部の皮膚に黒いしみができた場合には、自己判断せずに皮膚科を受診すべきです。
悪性黒色腫は表皮で発生しますが、増殖して真皮に入り込むと転移が起きるようになります。真皮にはリンパ管や血管が通っているため、そこからがん細胞が流れていってしまうのです。悪性黒色腫の転移は、約8割はリンパ行性転移で、血行性転移は2割程度です。
ダーモスコピー検査で表皮の中まで観察する
悪性黒色腫の診断と治療は、基本的に「悪性黒色腫の診療アルゴリズム」に従って行われます(図3)。
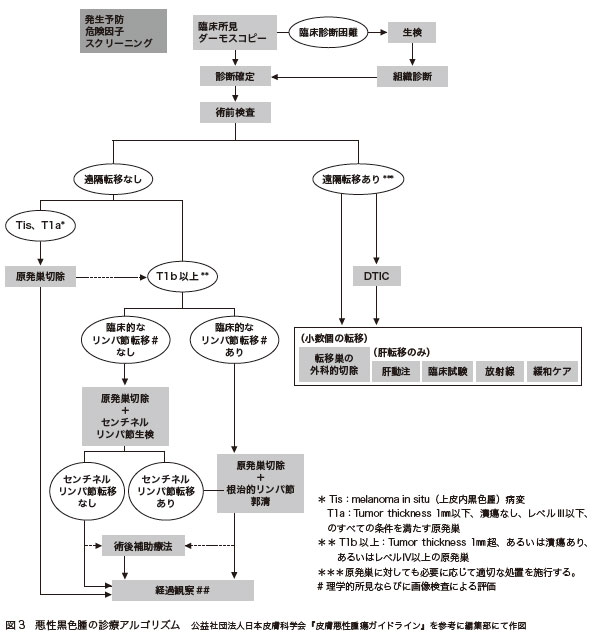
悪性黒色腫が疑われる場合に、まず行われる検査はダーモスコピー検査です。皮膚に超音波検査のときに用いるゼリーを塗り、特殊な皮膚用の拡大鏡を押し付けるようにして患部を観察します。10倍くらいに拡大できるのに加え、表皮の中の構造まである程度見ることができます。メラニンも見えますし、血管があればその状態までわかります。それによって、悪性黒色腫かどうかをほぼ判定することができます。
ダーモスコピー検査ではっきりしない場合には、生検が行われます。組織の一部を採取し、それを顕微鏡で調べる病理検査を行うのです。局所の麻酔をした後、パンチバイオプシーという患部を小さくくり貫く機械を使用し、組織を採取します。直径4㎜程度あれば十分に調べることができます。
悪性黒色腫は生検のために腫瘍に切り込むと、転移を誘発すると言われてきました。しかし現在では、生検を行って悪性黒色腫と診断がついた場合でも、1カ月以内に手術をすれば問題ないことが明らかになっています。悪性黒色腫である可能性が高い場合には、手術の予定を組んでおいてから生検を行います。生検をしてはいけないケースはほぼありません。
がんと診断がついた場合は、進行の程度を調べる必要があります(表1)
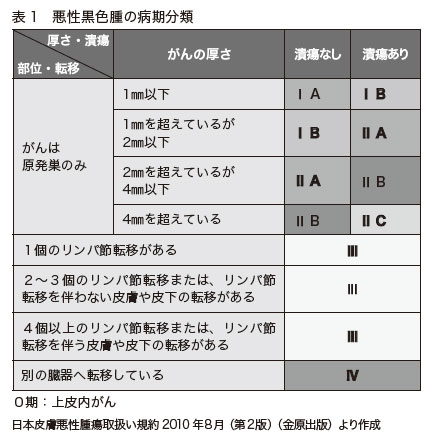
それを知るために、がんの厚さを調べます。生検を行うときに、できるだけ深くまで達していそうな部分を採取します。しかし、全体を調べないとわからないこともよくあります。
転移している可能性がある場合には、CT検査、PET検査を行い、転移があるかどうかを調べます。リンパ節や離れた臓器に転移巣が見つかることがあります。ただし、これらの画像検査で転移巣が見つからなくても、微小ながんが転移している可能性はあります。
それを見逃さないために、センチネルリンパ節生検が行われます。がんが原発巣からリンパ流に乗って出ていくとき、最初にたどり着くリンパ節をセンチネルリンパ節といいます。手術時にこのリンパ節を探し出して採取し、病理検査を行います。ここに転移がなければ、転移の可能性が少ないと判断できるのです。
センチネルリンパ節を特定するため、手術前日に放射性同位元素を原発巣周囲に注入し、手術時には色素を注入します。これらがどこに流れていくかを調べることで、センチネルリンパ節を特定するのです。採取したリンパ節の病理検査に数日を要するため、検査結果は手術後に明らかになりま
す。
がんの辺へ んえん縁から1~2㎝離して切除する
悪性黒色腫の治療では、離れた臓器への転移がなければ手術が行われます。がんを取り残さないために、がんの辺縁から距離をとって切除する必要があります。その距離は1~2㎝で、がんの厚さによって判断します(表2)。

指は脂肪層が少ないため皮膚と骨が近く、一部を切断しなければならない場合もあります。骨に浸潤しているケースもあるからです。そのような場合、多くは関節から先を切断する関節離断術が行われます。
切除した部位には、基本的に植皮が行われます。植皮には、鼠そけいぶ径部や鎖骨上部から採った皮膚が使われます。
リンパ節への転移がなければ、手術は原発巣を切除して終わりです。手術前に画像検査などでリンパ節転移が見つかっていた場合には、原発巣の切除に加えてリンパ節郭かくせい清* も行われます。原発巣の手術時にセンチネルリンパ節生検を行い、その結果、リンパ節転移があると判定された場合には、リンパ節郭清のための手術が改めて行われます。
郭清するリンパ節は、がんのできている部位によって異なります。足のがんなら鼠径部のリンパ節、手のがんなら腋のリンパ節です。背中のがんだと、腋と鼠径部のどちらにも転移することがあります。
悪性黒色腫の治療は手術が基本ですが、機能の温存や整容性を考慮して、手術以外の方法が選択されることもあります。たとえば、目にできた悪性黒色腫は、手術をすれば眼球を摘出することになります。鼻の粘膜や口腔粘膜にできた悪性黒色腫は、手術で切除すると顔の形が変わってしまいます。このような場合には、重粒子線治療や陽子線治療などの放射線療法が優先されることもあります。ただし、これらの治療は必ずしも標準治療ではなく、健康保険は適用されません。
手術後の再発を防ぐための補助療法として、化学療法が行われることがあります。抗がん剤のダカルバジンとインターフェロンを併用するDフェロン療法、インターフェロンを続けて打つインターフェロン維持療法といった方法があります。
離れた臓器に転移がある場合、それが単発なら放射線療法を行うことがあります。悪性黒色腫は放射線に対して感受性が低いのですが、ガンマナイフやトモセラピーのように、がんを焼き尽くすような治療が行われています。
*リンパ節郭清:リンパ節を切除す ること。
急速に進歩した分子標的薬と最新の免疫療法
悪性黒色腫で離れた臓器に転移がある場合、かつては有効な治療法がありませんでした。ところが最近になって、2つの有効な治療法が登場してきました。1つが分子標的薬、もう1つが免疫チェックポイント阻害薬です。
分子標的薬は、特定の遺伝子変異を持つ悪性黒色腫に効果があります。悪性黒色腫の治療に使われているベムラフェニブとダブラフェニブは、BRAF阻害薬というタイプの薬で、BRAFという遺伝子変異がある悪性黒色腫に効果を発揮します。そのため、まず遺伝子の検査が必要です。がんの組織を検査して、BRAF遺伝子変異が見つかれば、これらの薬を使用することができます。
BRAF遺伝子変異が陽性になる確率は、欧米人に多い表在拡大型では高いのですが、日本人に多い末端黒子型では1~2割と低いことがわかっています。多くの患者さんが治療対象とならないのです。
この2つの薬以外に、トラメチニブという分子標的薬があります。この薬はダブラフェニブと併用することで有効性を発揮します。
分子標的薬は、使用できた場合には非常によく効きます。短期間のうちにがんが縮小したり、肉眼的に消えてしまったりすることもあります。しかし、その効果はいつまでも続かず、多くは半年から1年ほどで耐性ができ、再びがんが増殖してしまいます。
もう1つの免疫チェックポイント阻害薬は、免疫の力を利用する薬です。免疫細胞は、体内のがん細胞を攻撃して死滅させる力を持っていますが、がん細胞はその攻撃を逃れる仕組みを持っています。その仕組みを働かなくさせることで、本来の免疫の力でがんを攻撃させるのが免疫チェックポイント阻害薬です。
現在、日本で悪性黒色腫の治療に使用できる免疫チェックポイント阻害薬は、ニボルマブ、イピリムマブ、ペンブロリズマブの3種類です。これらは、分子標的薬と違い、根治不能な悪性黒色腫であれば誰でも使用できます。
免疫チェックポイント阻害薬も非常によく効きますが、分子標的薬の効き方とは異なっていて、がんが急速に縮小したり、消えてしまうことは少ないです。しかし、がんの進行を抑えることが多いのです。悪くならずに維持するのにはよい薬です。
離れた臓器に転移があり、根治的な手術ができない悪性黒色腫では、まずBRAF遺伝子変異を調べ、陽性なら分子標的薬を使用します。そして、それが効かなくなる前に、免疫チェックポイント阻害薬に切り替えることが推奨されています。
悪性黒色腫の治療後の経過観察は、ステージⅠとステージⅡなら、3カ月に1回で、これを2~3年続けます。それ以降は6カ月に1回にします。ステージⅢ以上の場合は毎月で、3~5年は継続します。悪性黒色腫は再発しやすいので、経過観察のため頻繁に医療機関を受診する必要があります。
【有棘(ゆうきょく)細胞がん】
やけどや傷のあった部位にできることが多い
有棘細胞がんは、表皮の有棘層を構成している細胞が悪性化したものです。細胞が傷つけられることが原因となることがよくあります。そのため、やけど、外傷、放射線照射による炎症などがあった部位から発生することが多いのが特徴です。因果関係がはっきりしていることが多いがんなのです。やけどやけがをした後、30年も40年もたってから出てくることもよくあります。
このがんには、特徴的な症状はありません。結節* ができることもあれば、潰瘍化*することもあります。
*結節:皮膚にできるクルミ程度の隆起物。
*潰瘍化:皮膚などに欠損部が形成されること。
生検を行い必要に応じて画像検査を行う
有棘細胞がんの診断と治療は、基本的に「有棘細胞がんの診療アルゴリズム」に従って行われます(図4)。

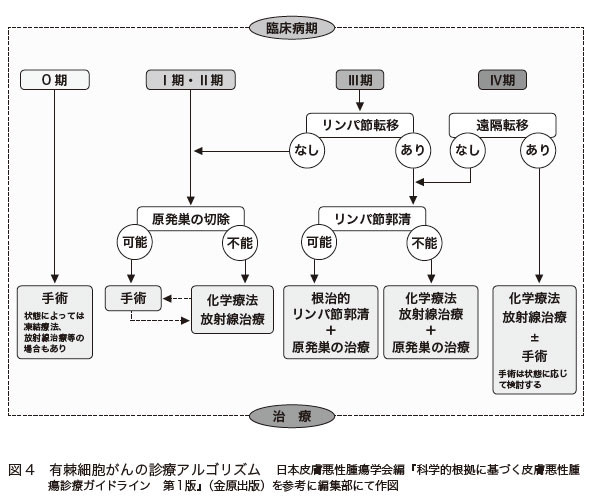
有棘細胞がんは潰瘍化したり、表面が崩れている場合は、ダーモスコピー検査は行いません。肉眼で観察し、すみやかに生検が行われます。それによって診断を確定します。
リンパ節転移や遠隔転移を調べるために、画像検査を行うことがあります。
原発巣を切除しリンパ節郭清は行わない
有棘細胞がんの手術では、がんの辺縁から1~2㎝離して切除します。リンパ行性の転移が少ないがんなので、再発を予防する目的でリンパ節郭清を行うことはありません。画像検査の結果、リンパ節が明らかに腫れているような場合にのみ、リンパ節郭清が行われ
ます。
有棘細胞がんは、治療せずに放置すると巨大な腫瘍になることがあり、そのような場合には、体の一部を切断しなければならないこともあります。
転移があり根治的な手術ができない場合や、手術後の再発予防に、化学療法や放射線療法が行われます。
有棘細胞がんは扁平上皮がんなので、他の扁平上皮がんと同じような化学療法が行われます。よく使われるのは、ペプレオマイシンとマイトマイシンを併用するPM療法です。その他、シスプラチンとドキソルビシンを併用するCA療法が行われることもあります。
放射線療法も併用しますが、角化が強いタイプ(分化度* の高いタイプ)の有棘細胞がんにはあまり有効ではありません。よく効くのは角化が弱いタイプです。
治療後の経過観察は、がんを手術で取り切れているなら、3カ月に1回程度です。それを2~3年続け、それ以降は6カ月に1回にします。
*分化度:細胞の成熟度合い。
【基底細胞がん】
ほくろと間違えやすい黒く小さい結節が特徴
基底細胞がんは、表皮の基底層の細胞ががん化したものではありません。がん細胞が基底細胞に似ているため、基底細胞がんと呼ばれています。黒光りしたような小さな結節をつくるため、最もほくろと間違われやすい皮膚がんです。大きくなると表面が崩れて潰瘍化することがあります。
基底細胞がんは、できている部位と大きさから、高リスク、中リスク、低リスクに分類されます。大部分が低リスクです。低リスクの場合、局所で大きくなることはありますが、転移することはほとんどありません。そのため、このがんで死亡する人はほとんどいません。
ダーモスコピー検査で悪性黒色腫と鑑別
基底細胞がんの診断と治療は、基本的に「基底細胞がんの診療アルゴリズム」に従って行われます(図5)。

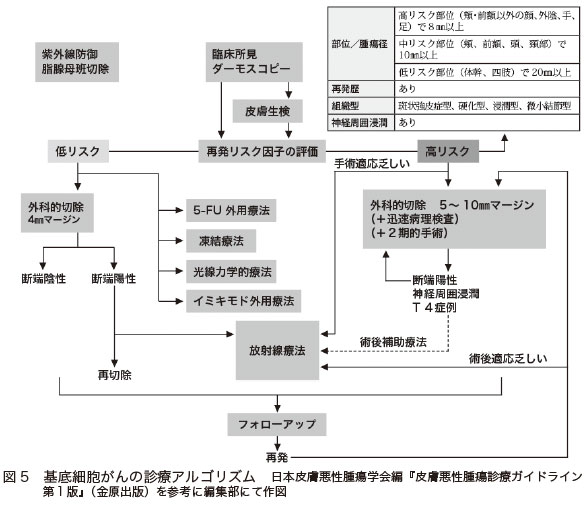
検査で重要なのはダーモスコピー検査です。表皮内のメラニンの状態を見ることができ、悪性黒色腫との鑑別が可能です。ダーモスコピー検査で基底細胞がんと診断がつけば、生検を行わずにすみます。ダーモスコピー検査ではっきりしない場合のみ、生検を行います。ダーモスコピー検査が行われるようになる前は、基底細胞がんの全例で生検が行われていましたが、現在は生検を行うほうが少なくなっているほどです。
原発巣を切除する
基底細胞がんの治療は手術が基本です。多くは転移しないので、原発巣を切除すれば治癒します。リンパ節郭清が必要になることはほぼありません。
切除する大きさによって、植皮や皮ひべん弁が行われます。植皮は他の部位の皮膚を採ってきて貼り付ける方法です。皮弁は、切除した部位の近くの皮膚を、脂肪組織や血管と一緒に、切除部位に移動させる方法です。皮弁なら皮膚の色や質感が近いので、きれいに仕上がります。
ただ、皮弁は厚いため、局所再発した場合に発見が遅れるという問題があります。基底細胞がんは確実に切除できていれば再発のリスクが低いため、顔の手術などでは皮弁が行われることがあります。
治療後の経過観察は、手術でしっかり取り切れている場合は、1年間は3カ月に1回ですが、それ以降はセルフチェックとします。それだけ再発のリスクが低いのです。
【乳房外パジェット病】
乳頭部に発症する乳房パジェット病と、それ以外の部位にできる乳房外パジェット病があります。この2つはまったく別の病気で、乳房パジェット病は乳がんの一種、乳房外パジェット病は皮膚がんの一種です。
乳房外パジェット病が発症するのは、アポクリン腺の多い部位で、腋、陰部、肛門周囲などです。それ以外の部位にできることもありますが、ごくまれです。基本的にはアポクリン腺のある部位で発生し、表皮内で増殖します。
それが進行し、基底膜を越えて真皮に入ると、主にリンパ液の流れに乗って転移していきます。血行性の転移は少なく、8割以上がリンパ行性転移です。
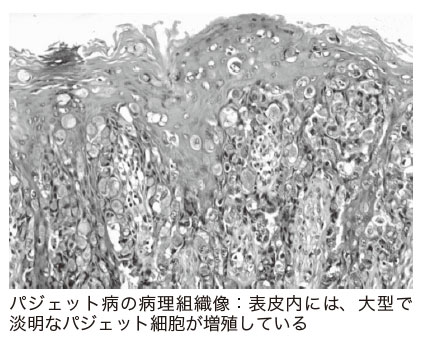
現れる症状は、湿疹や真菌症とまぎらわしい皮膚症状で、赤くてカサカサした感じになります。色素沈着する場合と色素が抜ける場合があります。進行すると、結節や腫瘤を呈する部分が現れてきます。また、かゆみがあります。
生検によって診断を確定させる
乳房外パジェット病の診断と治療は、基本的に「乳房外パジェット病の診療アルゴリズム」に従って行われます(図6)。
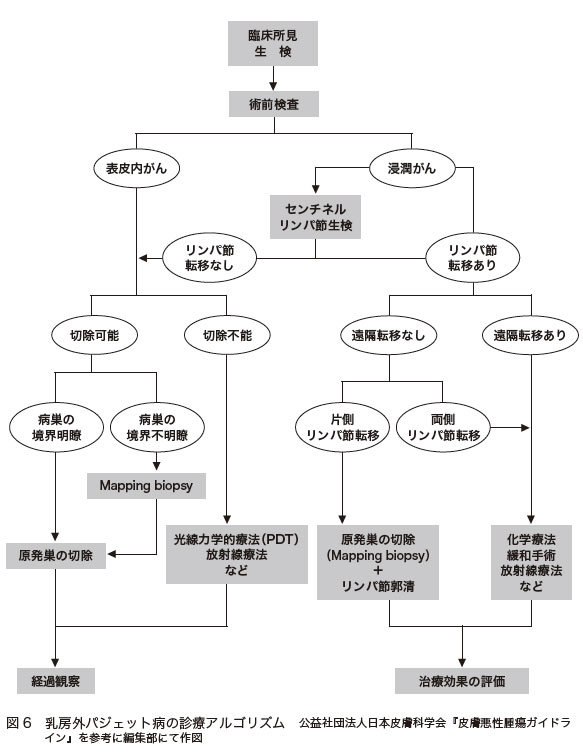
このがんでは、ダーモスコピー検査を行っても、あまりよくわかりません。乳房外パジェット病であると診断するためには、生検が行われます。
手術が基本だが放射線療法も効果が高い
原発巣の手術が治療の基本となっています。ただ、がんの辺縁からどのくらい離して切除するかについては、必ずしも定説はありません。1㎝でいいという説もあれば、もっと広くとるべきという意見もあります。もともと肉眼的境界がはっきりしていない、という難しさもあります。
手術は原発巣の切除が基本で、再発予防のためにリンパ節郭清を行うことはありません。リンパ節が腫れていて、転移が明らかな場合だけリンパ節郭清が行われます。
放射線に対する感受性は悪くないので、根治が望めない場合などに、放射線療法は行われます。また、肛門周囲などに発症し、人工肛門を造設したくない人が、放射線療法を選択するようなケースもあります。比較的初期の病変では、手術をせずに、放射線療法だけで治癒してしまうこともあります。
化学療法は、腺がんに準じて行います。まずタキサン系抗がん剤のパクリタキセルやドセタキセルが使われます。それに続き、5–FUとシスプラチンを低用量で投与する低用量FP療法が行われることもあります。
治療終了後の通院ですが、広い範囲を切除した場合には、機能面での問題が生じることがあります。陰茎や陰嚢の手術では排尿障害が、肛門周囲の手術では排便障害が起きたりします。そのために、2カ月に1回くらい通院してもらうことがよくあります。そういった問題がなければ、3カ月に1回程度にします。











