進歩する「新時代のがん免疫治療」
─ 免疫抑制からの脱却による「がん治療の展望」 ─
埼玉医科大学国際医療センター 消化器病センター消化器腫瘍科 教授
(2013年.vol10)
急速に進歩するがん免疫治療
私たちの体の中には、ウイルスや病原体、がん細胞などの異物を攻撃する働きが備わっています。この作用は「免疫」と称されています。
がん治療の分野では、この免疫の働きを担う免疫細胞を増強して、がん細胞を排除することを目指した、がん免疫治療法が開発されてきました。この治療法は、外科的手術・抗がん剤治療・放射線治療に次ぐ第4のがん治療とも言われ、さまざまなものが存在しています。
古くは生体の免疫作用を高める作用を持つ免疫賦活剤が脚光を浴びたこともありました。そして、患者さんの体内から採取した免疫細胞を増強・活性化させて点滴で体に戻す免疫細胞療法も多く実施されてきました。
さらに近年では、免疫の研究が急速に進展し、「その患者さんのがん細胞だけを狙い打ちして攻撃する免疫細胞」が特定されるようになりました。しかも、そのがん細胞を攻撃できる免疫細胞は、がんに罹患した患者さんの体の中にも確実に存在していることが明らかになったのです。そこで、この特定された免疫細胞を増強・活性化させるために、より進化した免疫細胞療法や新たにワクチン療法が開発されるようになってきました。このように、免疫学・遺伝子工学・分子生物学の進歩に伴い、がんに対する免疫療法は画期的な発展を遂げたのです。その一方で、臨床現場では、その最新の免疫療法においても思うような効果が得られていないという実状もあります。
免疫抑制の解除・軽減が治療効果向上のポイント
我々も、以前より免疫細胞療法の研究を行ってきましたが、なかなか十分な効果が現れませんでした。そこで、なぜ患者さんの免疫がうまくがん細胞を攻撃してくれないのかを調べる研究をしてきました。その結果、がんの進行に伴い、患者さんの全身では炎症反応が強くなり、栄養状態も悪化し、がんに対する免疫機能がうまく働かなくなっていることが判明してきたのです。そして、最近になって、この免疫機能の低下の原因が、がんの患者さん特有の状態である「免疫抑制」にあることが多くの研究結果からわかってきました。
免疫抑制状態になると、いくらがん患者さんの免疫細胞を活性化させても、肝心の体内の免疫細胞の働きが抑制・無力化されてしまって、がん細胞への攻撃が不能な状態となってしまいます。つまり、せっかくの免疫療法の効果も乏しいものになってしまうのです。それが、臨床現場では思うような効果に結び付いていない大きな要因となっていると言えるでしょう。
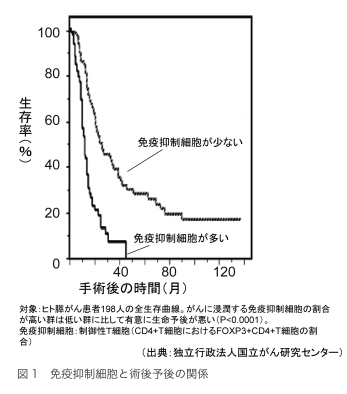
さらに、免疫の抑制状態に陥ったがん患者さんの体内では、「免疫抑制細胞(制御性T細胞や骨髄由来免疫抑制細胞)」と呼ばれる細胞が異常に増えることで、免疫細胞の機能が抑え込まれて、免疫細胞自体の活性も損なわれてしまうこともわかってきました。実際に、免疫の抑制状態に陥って、免疫抑制細胞が多くなった患者さんほど標準治療後の生存率が悪くなるという臨床データも報告されるようになってきています(編集部注 図1参照)。したがって、免疫抑制の主な原因の1つが免疫抑制細胞の異常な増殖にあり、それを食い止めることで予後が改善する可能性も高まると考えられます。
このように、免疫抑制を解除・軽減してがんの治療効果を向上させようというものが、がん治療の大きなポイントとなってきたのです。
免疫抑制を解除・軽減する
治療法の開発が進む
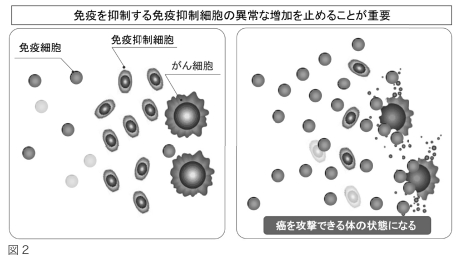
先述のようにがん治療における「免疫抑制」の問題が認識されてきました。そして、がん患者さんが免疫力を発揮させて治療効果を高めるためには、免疫抑制の解除・軽減が重要だとわかってきました(図2参照)。
既に、免疫抑制を解除し、がん細胞に対する免疫の働きを強化させる抗がん剤の開発も進められています。2011年には米国食品医薬品局(FDA)から進行期の悪性黒色腫に対する分子標的薬としてイピリムマブという薬剤が最初に承認を受けています。この薬剤には免疫反応を抑制する働きがある分子(CTLA-4)をブロックし、免疫細胞のがんに対する攻撃力を回復させる作用があります。また、イピリムマブは、前立腺がんや肺がんなどへの適用拡大が模索されています。
その他に、直に免疫細胞に働く分子標的薬として、トレメリムマブの進行性悪性黒色腫を対象とした第3相臨床試験が行われています。この分子標的薬もイピリムマブ同様にCTLA-4の阻害薬です。さらに、やはり免疫細胞に直接働いて免疫細胞の活性を回復させる抗PD‐1抗体やがん細胞の表面にある免疫抑制分子をブロックするPD‐L1抗体については、非小細胞肺がん・腎細胞がんなど様々な癌種を対象とした第1相試験が行われています。これらの分子標的薬については、本年の米国臨床腫瘍学会でも新しい臨床データが報告されるなど、現在非常に注目が集まっています。
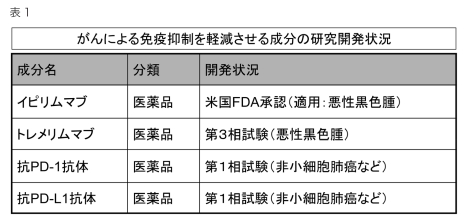
また、これらの分子標的薬は、がん患者さんの体内で起きている免疫抑制状態を解除し、体の中に元々ある、がんを攻撃する免疫細胞の機能を回復させる作用を持っています。そして、その免疫の働きだけで、治療効果を獲得していると考えられるのです。つまり、免疫抑制を解除するだけでも、抗がん剤や放射線などを用いたがんの標準治療の効果を高められる、という証明にもなったのです(表1参照)。
現在、こうした分子標的薬は日本では承認されていません。また、仮に日本で承認されたとしても、しばらくは限られたがん種の患者さんにしか使用することができず、かつ高額の費用を要してしまう可能性もあります。
今後は、最先端のがん免疫治療であるワクチン療法や免疫細胞療法においても、免疫抑制の解除は、治療法の効果をさらに高めるキーポイントになってくるに違いありません。
免疫療法に関しては、ワクチン療法・細胞療法のいずれも、先述の免疫抑制を解除する方法と併用し、より効果を高める流れになると推測できます。また、古くから「手術をした患者さんの予後は免疫能で左右される」と言われていますが、免疫抑制を解除して免疫機能を正常へと改善することが、標準療法である外科的手術や抗がん剤治療などの効果を高める可能性を十分に含んでいます。
免疫細胞療法に関しては、抗がん剤と比較して腫瘍の縮小効果などのエビデンスが乏しいのは否めませんが、これまで免疫細胞療法に取り組んできた医師たちの治療結果を長いスパンで見ますと、抗がん剤治療単独の場合と比較し、併用したほうが予後の改善が図られることがわかってきました。そこに、今回、私が述べた「免疫抑制に対する治療」が確立されれば、免疫細胞療法の効果がさらに向上し、改めて評価されるようになるのかもしれません。
その他にも、薬剤ではないですが、天然由来の有用成分で、「免疫抑制」の研究成果を積み重ねている日本の製薬企業もあります。そこで研究されている有用成分がシイタケ菌糸体抽出物(編集部注:詳しくはこちらの記事)です。
シイタケ菌糸体抽出物は、ヒト臨床研究において、免疫抑制細胞の異常な増加を抑える作用が報告されています。今後、ヒトでの効果がより詳細に明らかにされてくるのではないかと思います。
今後、これらの免疫療法を組み合わせた治療法が確立されることで、「免疫抑制」を解除・軽減させ、患者さんが本来持っている免疫でがん細胞に向かい合える体の状態にしていくことが可能になると考えられます。
多くの医療者が取り組みはじめる免疫抑制の解除
患者さんの体の状態という点では、先述のように免疫抑制と患者さんの栄養状態や全身の炎症反応は密接に関係しています。栄養状態が悪い患者さんは、炎症反応が高く、抗がん剤の効果が乏しく、予後が悪いこともわかってきています。
まだヒトで証明し切れてはいないものの、栄養状態や炎症反応を改善することも、免疫抑制の改善につながる可能性もあります。とりわけ、栄養状態の改善は、がん患者さんにとって負担が少ない方法です。したがって、がん患者さんに適切な栄養を摂取してもらうことが、免疫機能の回復を図って治療効果を増強させる、という治療の方法も注目され始めています。
現在、従来の「免疫の活性化」だけを重視するのではなく、「免疫抑制の解除」の重要性も多くの医療者に認識されるようになってきました。こうした基盤が構築されたうえで、がん治療の効果を高め、より多くの患者さんにメリットをもたらすことを目指して、免疫抑制を解除する研究は積み重ねられているのです。











