第77回日本癌学会学術総会レポート
がん治療における”内なる”免疫力の重要性
免疫療法が第4の治療法として注目を集める
2018年9月27~29日、大阪国際会議場とリーガロイヤルホテル大阪にて、第77回「日本癌学会学術総会」が開催された。日本癌学会は、がん研究の発達を図る目的で、がんの基礎研究から臨床研究まで、幅広い研究に関係する学会である。

第77 回日本癌学会学術会は大阪国際会議場(リーガロイヤルホテル大阪)において行われた
昨今の海外の学会、特にがんの治療を扱う臨床腫瘍学の学会では、手術、薬物療法、放射線療法に続く第4の治療法として、免疫療法が注目を集めている。免疫チェックポイント阻害抗体療法の出現により、免疫療法はがん治療の重要な一つに加えられることになった。今回の学術総会でも、免疫療法に関わるさまざまな研究が発表されていた。多岐にわたる研究結果が報告されていたが、その中に島根大学医学部の原田守教授による「がん治療における”内なる”免疫力の重要性」と題する講演があったので紹介しておきたい。

講演中の原田守教授
がん免疫療法では、患者の体内に生じたがん抗原(※1)を認識するT細胞(※2)の機能を回復させることが主な機序となっている。また、免疫療法が引き金となって、患者自身の免疫応答が引き起こされることが、その後の治療効果にも関わっていることも明らかになってきたようだ。
※1 がん抗原とは、がんに存在する特有のタンパク質のこと。体が「異物 (敵)」と判断する目印。
※2 T細胞とは免疫細胞の一種。
最近のがん免疫療法が明らかにしたこと
がん免疫療法で、がん細胞を攻撃する中心的な役割を果たすのはT細胞である。がん局所でがん細胞が放出したがん抗原を樹状細胞という免疫細胞が橋渡しして、T細胞がそのがん抗原を認識することで、抗がんT細胞が誘導され、その抗がんT細胞が、がん細胞を傷害することになる。
T細胞が認識するがん抗原はさまざまで、がん・精巣抗原「MAGE、NY–ESO–1」、分化抗原「メラノサイト分化抗原(MALT1)、前立腺関連抗原(PSA)」、種々のがん細胞に高発現情報する抗原「WT–1、p53、HER2」、ウイルス抗原「HPV(子宮頸がん)、HTVL–1(成人T細胞白血病)」、胎児性抗原「CEA、AFP」、変異抗原「アミノ酸の変異に伴う遺伝子変異、BRAF」などがある。
T細胞がこうした抗原を認識し、抗がんT細胞が誘導されることが、免疫療法では重要である。そういう意味で、がんの免疫療法は、患者自身の体の中で、抗がんT細胞を誘引するような内因性の免疫応答が起きているかどうかがカギを握っている、と言えるだろう。治療する側は、免疫応答を回復させたり増幅させたりすることで、治療に結びつけることが重要なのである。
内因性の免疫応答を引き起こした例
内なる免疫応答が治療効果に影響を及ぼすことを示す2つの例がある。
IL–12(インターロイキン12)を投与した担がんマウスモデル
メラノーマ(※1)を接種したマウスを対象に、免疫細胞を活性化させる働きを持つサイトカインのIL–12を投与する群と、投与しないコントロール群で、その後のがんの状態を調べた。
コントロール群では腫瘍が増殖していくが、IL–12投与群では投与終了後も、長く腫瘍の増殖が抑えられる(図1)。このマウスの体内で何が起きているのかを調べた。
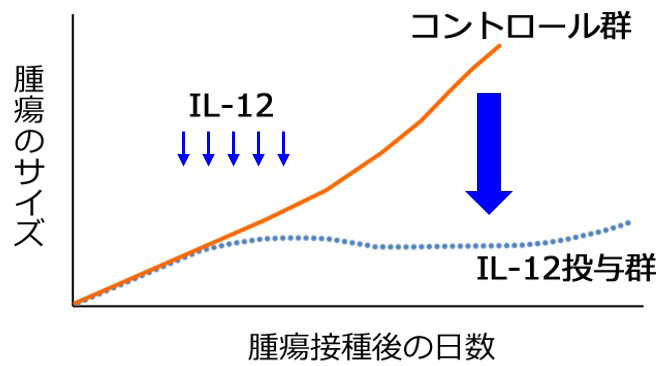
図1 IL–12 投与によるがん増殖抑制効果
効果が持続しているマウスでは、投与された外因性のIL–12によって、体の中で内因性のIL–12が産生されていることが考えられた。IL–12が産生されたとすれば、その場は局所リンパ節である。局所リンパ節を郭かくせい清(※2)する実験も行った。郭清すると内因性のIL–12の産生がなくなり、腫瘍の増殖を抑えられないことを確認した。この研究は、腫瘍の増殖が抑えられたのは、IL–12により抗がんT細胞の誘導サイクルが回り始めたためであることを示唆している。
※1 メラノーマ(悪性黒色腫)とは、皮膚がんの一種。
※2 リンパ節の郭清とは、リンパ節を手術などで取り去ること。
がんペプチドワクチンを受けたがん患者
前立腺がんでペプチドワクチン治療を受けた患者の例が報告されている。ペプチドの投与でいったんPR(部分奏効)となったが、その後PD(進行)となった。効果が現れたときの抗体の状態を調べると、PSAたんぱく(※)に対して抗体が誘導されていたことがわかった。PSAペプチドの投与から最終的には、PSAたんぱくに対するT細胞の反応性が拡大し、抗がんT細胞が誘導されていたことが示されている。
※PSAたんぱくとは、前立腺特異抗原のこと。
がんの免疫療法にはいろいろな種類があるが、内なる免疫応答のことを考えると、化学療法や放射線療法も免疫療法と考えることができる。化学療法に関しては、抗がん剤が細胞傷害作用でがん細胞を殺すだけでなく、抗がん剤で樹状細胞が活性化し、がん抗原を取り込んで、結果的にがん特異的なT細胞を誘導することが知られている。
放射線療法に関しては、アブスコパル効果が知られている。ある局所のがんに放射線を照射すると、離れた部位のがんにも効果が現れる。これも、放射線によって抗がんT細胞が誘導されるためであると考えられている。がん治療における免疫療法の位置づけを整理しておく必要がある(図2)
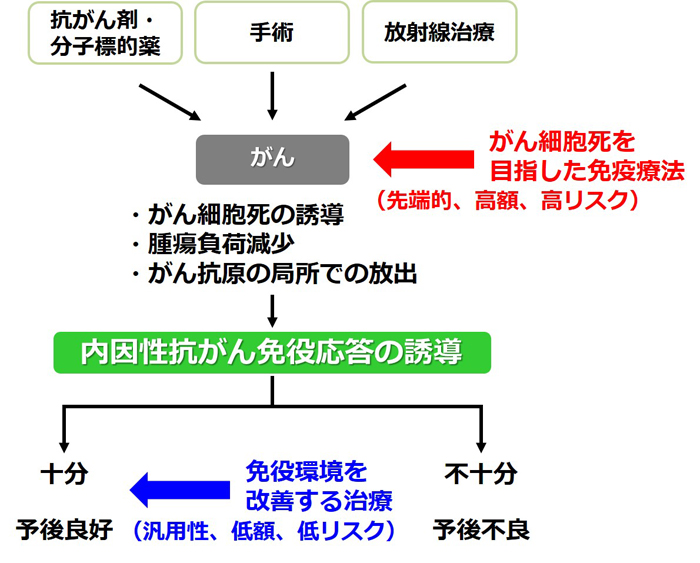
図2 がん治療における免疫療法の位置づけ
注目を集めているのは、免疫チェックポイント阻害抗体療法など、がん細胞死を目指した先端的な治療である。しかし、その治療を行って残ったがん細胞に対しては、内因性抗がん免疫応答が誘導されることが重要である。それが十分に誘導されるかどうかが、予後に大きく影響する。そこで、先端的な免疫療法とは別に、がん患者の免疫環境を改善する治療にも大きな意味があると考えられるのである。
シイタケ菌糸体抽出物の免疫応答修飾効果
シイタケ菌糸体の経口摂取により、次のような効果が現れ、体内の免疫環境が改善することが明らかになっている(表を参照)。
| タイトル | 方法 | 結果概要 | 報告 |
| 免疫抑制細胞(Treg)減少による免疫環境の改善作用 | がん細胞を移植したマウスに、シイタケ菌糸体エキスを経口投与した。 | シイタケ菌糸体エキス投与群では、Treg 細胞数が減少して免疫環境が改善し、がんの増殖も抑えられた。 | Cancer Science誌 2011年 |
| 免疫抑制細胞(Treg)減少による免疫環境の改善に伴うペプチドワ クチンの抗がん作用増強効果 |
がん細胞を移植したマウスに、シイタケ菌糸体エキスとペプチドワクチンを併用して投与した。 | ペプチド投与のみのマウスに比べ、シイタケ菌糸体エキスを併用したマウスではTreg 細胞が減少して、免疫環境が改善して抗がん作用が増強し、がんの増殖が抑えられた。 | Cancer Immuno Imm 誌 2012年 |
| がん移植によって炎症を抑えることによる免疫環境改善作用 | 大腸がん細胞を移植したマウスに、シイタケ菌糸体エキスを経口投与した。 | シイタケ菌糸体エキス投与群では、がんによる炎症が抑えられ、免疫環境が改善して抗がん作用が増強し、がんの増殖が抑えられた。 | Oncology Reports 誌 2012年 |
| 加齢に伴う慢性炎症の抑制による免疫環境改善作用 | がん細胞を移植した高齢のマウスに、シイタケ菌糸体エキスを経口投与した。 | シイタケ菌糸体エキス投与群では、がんによる炎症を抑えるのに加え、加齢による慢性炎症も抑えることで、免疫環境を改善し、がんの増殖が抑えられた。 | Cancer ImmunolImmunother 誌 2016年 |
表:シイタケ菌糸体抽出物の抗がん免役修飾効果
①免疫抑制細胞(Treg※)減少による免疫環境の改善作用
がん細胞を足底部に接種したマウスではがんの増殖に伴いTregが増殖し免疫環境が悪化する。このマウスにシイタケ菌糸体を摂取させると、Tregの増加が抑えられ、免疫環境が改善することで、がんの増殖が抑制される。このとき、局所リンパ節では、がんに特異的なT細胞が誘導され、がんに対する攻撃の指標であるインターフェロンγ(ガンマ)が高産生されていた。
※免疫抑制細胞(Treg)とは、免疫細胞の働きを抑制する働きをする細胞のこと。
②免疫抑制細胞(Treg)減少による免疫環境の改善に伴うペプチドワクチンの抗がん作用増強効果
がん細胞を足底部に接種したマウスを対象に、皮膚がんの代表的なペプチドであるTRP2をワクチンとして投与した群、シイタケ菌糸体を摂取した群、TRP2とシイタケ菌糸体を併用した群で、治療効果を比較した。その結果、ワクチンだけでも効果が現れるが、シイタケ菌糸体群ではそれを上回る効果があり、併用した群ではがんの増殖がさらに抑えられていた。
その機序を調べてみると、シイタケ菌糸体を摂取するだけで、がん局所でがん抗原に特異的なT細胞をある程度誘導できていた。一方、ペプチドでは一時的に反応が上がるが、それが持続していなかった。ワクチンとシイタケ菌糸体との併用ではシイタケ菌糸体による免疫環境の改善により、ワクチンによって誘導された抗がんT細胞を長期間にわたって高い状態に維持できることがわかった。
③がん移植によって炎症を抑えることによる免疫環境改善作用
マウスの盲腸壁に大腸がん細胞を移植し、シイタケ菌糸体を与える群と与えない群で比較した。
盲腸壁に大腸がん細胞を移植すると、血液中に炎症性サイトカイ
ンであるIL–6(インターロイキン6)が急激に増加する。体内にがんがあるのは、慢性的な炎症状態が続くことを意味するので、その炎症に伴ってIL–6が増加するわけだ。ところが、シイタケ菌糸体を摂取したマウスでは、IL–6の増加も抑えられ、がんの増殖も抑えられることがわかった。
④加齢に伴う慢性炎症の抑制による免疫環境改善作用
人間のがんが高齢者に多いことを考え、高齢のマウスを使った研究も行われた。若いマウスに比べ、加齢マウスでは血清IL–6が高くなることが知られているが、シイタケ菌糸体を摂取させると、この上昇をある程度抑えることができた。
若いマウスと加齢マウスの腹側に大腸がん細胞を移植し、大腸がんワクチンを投与するワクチン群と、ワクチンとシイタケ菌糸体の摂取を併用する併用群で治療効果を比較した。若いマウスではワクチン単独でも効果があり、抗がんT細胞も誘導されていた。シイタケ菌糸体を加えた併用群と、治療効果の差はほとんどなかった。しかし、加齢マウスでは、ワクチンだけでは不十分で、抗がんT細胞の誘導も十分には起こらなかった。ところが、シイタケ菌糸体を併用した群では、抗がんT細胞の誘導が高まり、ワクチンの効果を回復させて、がんの増殖も抑えられていた。
加齢またはそれに伴う慢性炎症は免疫環境を悪化させ免疫療法に対する大きな抵抗性となっている。それをいかに回復させるかが、免疫療法の効果を引き出すためにはとても重要だと考えられる。
まとめ
がんの第4の治療法として認められたがんの免疫療法だが、現在は、免疫チェックポイント阻害抗体療法など、がん細胞死を目指した治療が注目を集めている。その治療は非常に先端的だが、同時に高額でもある。また、かつて免疫療法は体に優しいと言われていたが、がん細胞死を目指した免疫療法では、重篤な有害作用が現れることもある。
免疫療法には、体内の免疫環境を改善することを目的とした治療も存在する。シイタケ菌糸体もその一つである。こうした治療は、汎用性があり、価格が低く、有害作用のリスクも低いといった特徴がある。がん患者の体内の免疫環境を整えるために、特に高齢の患者には有用であると考えられる。今後、ヒトを対象にした臨床試験などの研究が期待されている。










